Документ содержит актуальные научные данные и разработанные на их основе рекомендации по менеджменту аритмий, возникающих у пациентов, которые пребывают на лечении в отделениях интенсивной терапии (ОИТ). Особое внимание уделено подходам к стратификации рисков развития и видов аритмий у различных категорий пациентов, выбору наилучшей стратегии медикаментозного и немедикаментозного лечения на основе соотношения «риск-польза», а также менеджменту электронных кардиомодулирующих устройств. Авторы документа подчеркивают необходимость такого подхода для повышения скорости принятия клинических решений в условиях ОИТ. Ниже представлены основные тезисы консенсусного документа.
До начала антиаритмической терапии следует оценивать функцию почек и печени и соответственно подбирать дозу антиаритмического препарата (ААП), руководствуясь его конкретными фармакокинетическими свойствами.
При суправентрикулярных и желудочковых аритмиях правильный выбор ААП зависит от тщательной оценки гемодинамического статуса и коморбидных состояний.
Пациентам с критически нестабильной гемодинамикой показана немедленная электрическая кардиоверсия или дефибрилляция. После стабилизации состояния следует выявить и устранить обратимые причины нарушения гемодинамики.
Одновременное использование антиаритмической терапии и препаратов других групп, которые влияют на длительность интервала QT, требует большой осторожности и надлежащего мониторинга: если QT≥500 мсек, терапию ААП прерывают. Лечение ААП не рекомендовано пациентам с уже имеющимися QT≥500 мс, значительной дисфункцией SA или AV-узла без резервного кардиостимулятора на случай развития брадикардии.
У пациентов с черепно-мозговой травмой (ЧМТ) повышение внутричерепного давления вызывает чрезмерную активацию симпатического ответа, провоцирующего возникновение тяжелых аритмий. Для снижения частоты этих осложнений рассматривают применение β-адреноблокаторов.
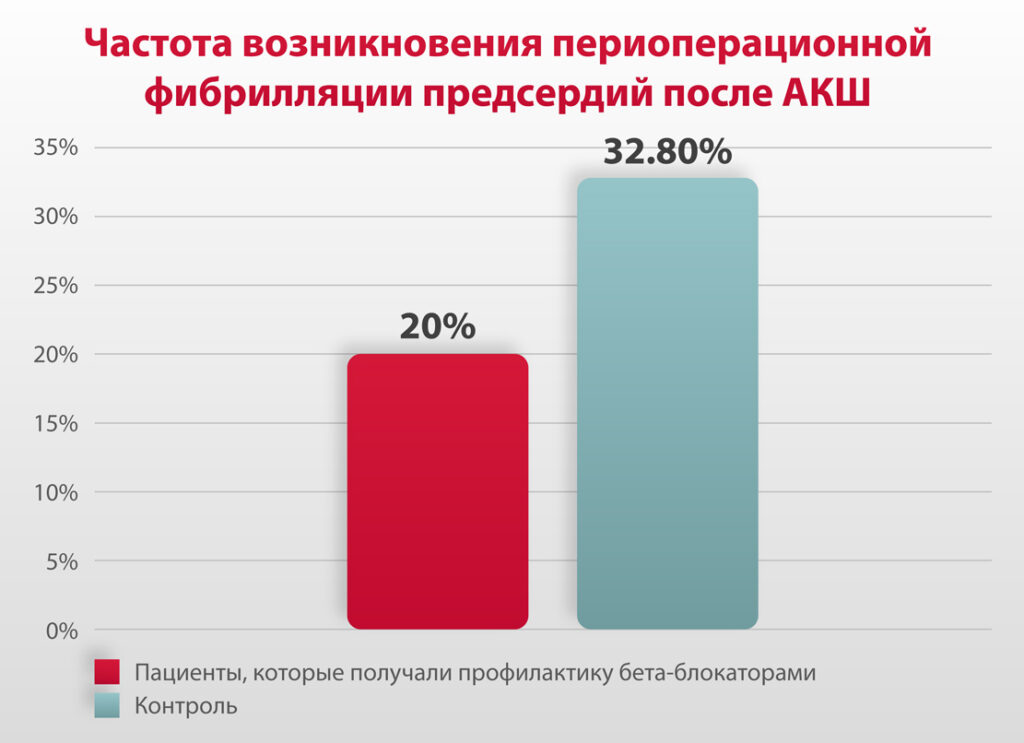
Профилактика β-адреноблокаторами после аортокоронарного шунтирования (АКШ) снижает частоту возникновения послеоперационной фибрилляции предсердий (ПОФП) с 32,8% до 20%. На основании этих данных пациентам после кардиохирургических вмешательств рекомендована периоперационная терапия β-адреноблокаторами.
При возникновении фибрилляции предсердий пациентам с нестабильной гемодинамикой показана электрическая кардиоверсия. При стабильной гемодинамике, после устранения возможных обратимых причин, для поддержания синусового ритма применяют β-адреноблокаторы.
β-адреноблокаторы (при хорошей переносимости) особенно эффективны для контроля острых нарушений ритма в условиях повышенного симпатического ответа у пациентов с аритмиями, а также при стабильной желудочковой тахикардии. В критических ситуациях предпочтительно введение эсмолола в силу его ультракороткого действия. При непереносимости β-адреноблокаторов или недигидропиридиновых Са-блокаторов применяют амиодарон. В качестве препарата третьей линии терапии используют дигоксин.
У пациентов после кардиологических операций для профилактики послеоперационной фибрилляции предсердий эффективны β-адреноблокаторы и амиодарон. При СН или гипотонии для контроля ритма можно рассматривать дигоксин, однако необходимо тщательно оценить риски развития аритмии.
У пациентов с ПОФП подходы к терапии базируются на оценке риска инсульта, тромбоэмболий и кровотечений по шкалам CHA2DS2VASc и HAS-BLED.
В заключение авторы также отмечают важность тщательной оценки и системного подхода для эффективного менеджмента аритмий в условиях ОИТ.